Sigue la polémica: Sociedad Argentina de Terapia Intensiva rechazó uso de suero equino aprobado por ANMAT, hablaron los especialistas
A través de un comunicado, aseguraron que no se recomienda "en los pacientes que requieren asistencia respiratoria mecánica y en los pacientes que hayan recibido plasma de convalecientes para Covid-19″.
Por Canal26
Lunes 18 de Enero de 2021 - 08:24
 Terapistas rechazan uso de suero equino.
Terapistas rechazan uso de suero equino.
La Sociedad Argentina de Terapia Intensiva (SATI) descartó la utilización del suero equino hiperinmune para tratar a los pacientes con coronavirus, práctica que había sido aprobada por la Anmat semanas atrás.
Generó la polémica y diferentes opiniones al respecto. A través de un comunicado, aseguraron que “debido a los resultados presentados en este estudio fase 2/3, la SATI recomienda fuertemente no utilizar suero equino hiperinmune en los pacientes internados en terapia intensiva, en los pacientes que requieren asistencia respiratoria mecánica y en los pacientes que hayan recibido plasma de convalecientes para Covid-19″.
Según informaron en el escrito, “no se demostraron los objetivos primarios y secundarios de eficacia clínica en ningún caso, no encontrándose diferencias significativas entre los pacientes que recibieron el suero equino hiperinmune y los que recibieron placebo, en relación al ingreso a terapia intensiva, requerimiento de asistencia respiratoria mecánica y de mortalidad”.
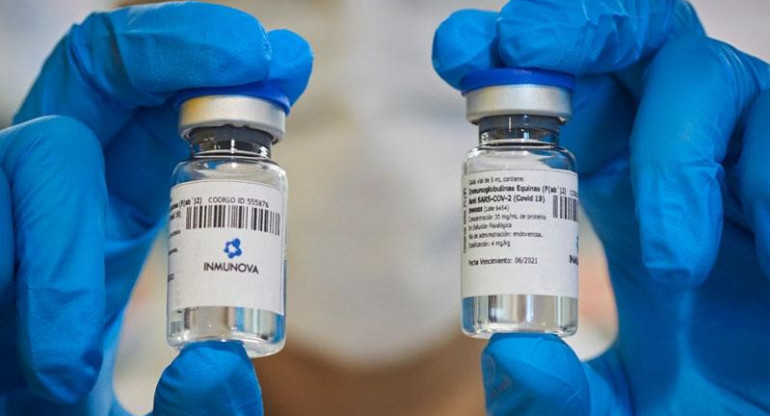
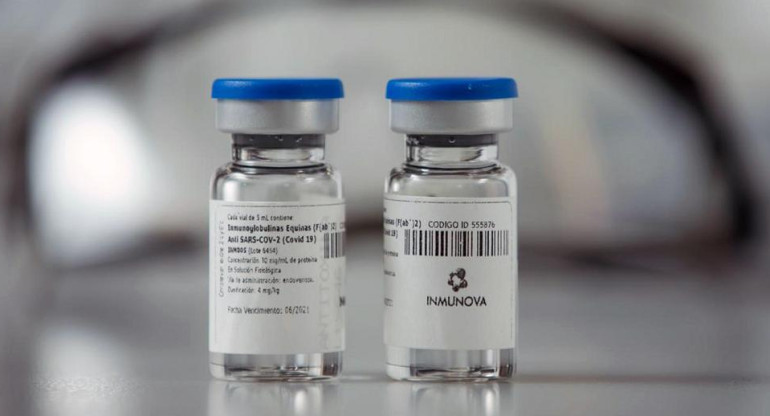
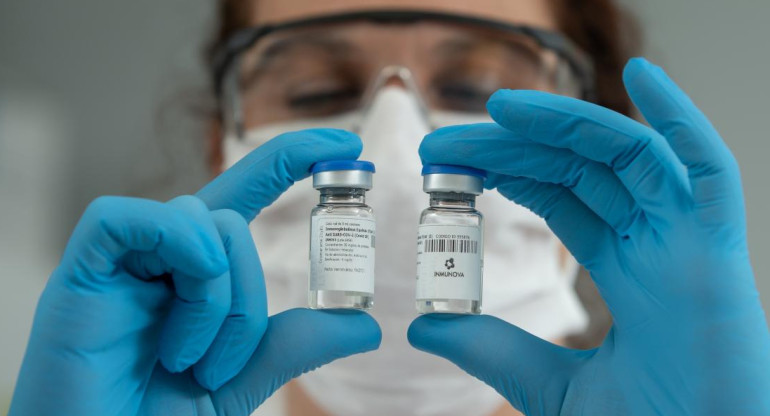
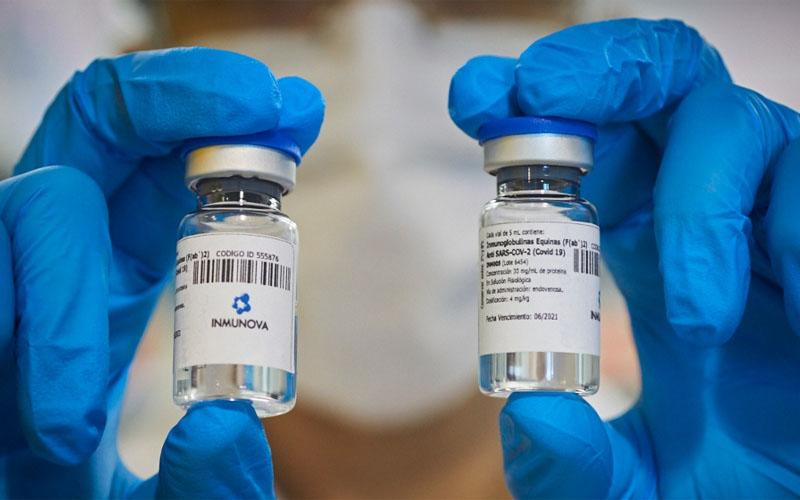 Suero equino, en medio de la polémica.
Suero equino, en medio de la polémica.
Los terapistas rechazaron la incorporación del producto por la falta de evidencia sobre sus beneficios. En ese sentido, aclararon que su posición “queda sujeta a posteriores modificaciones según el avance de los conocimientos y publicaciones científicas”.
Semanas atrás, la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat) había autorizado en diciembre la utilización del suero equino hiperinmune para tratar pacientes con coronavirus.
Aseguran que “la autorización bajo condiciones especiales se produce teniendo en cuenta los beneficios terapéuticos del producto. La agencia de regulación argentina otorgó una inscripción del medicamento en el REM con carácter condicional y por el plazo de un año. Está indicado para el tratamiento de pacientes adultos con enfermedad de curso moderado a severo”.
La discusión, que gira en torno de disquisiciones técnicas como "intervalos de confianza" (la variabilidad entre la medida obtenida en un estudio y la medida real de la población) y conceptos estadísticos como el "p-valor" (que indica la posibilidad de que el resultado de una prueba clínica se deba en mayor o menor medida al azar), escaló hasta tal punto que hace unos días la Sociedad Argentina de Terapia Intensiva emitió un comunicado en el que recomienda fuertemente "no utilizarlo en los pacientes internados en terapia intensiva, en los que requieren asistencia respiratoria mecánica, y en los que hayan recibido plasma de convalecientes". Y agrega: "De acuerdo con los datos presentados, no se demostraron los objetivos primarios y secundarios de eficacia clínica en ningún caso".
Al respecto, Elsa Baumeister, jefa del Servicio de Virosis Respiratorias del Instituto Malbrán, lo respaldó en el informe matutino del Ministerio de Salud de la Nación, diciendo que los resultados mostraron 45% de reducción en la mortalidad, 24% en necesidad de derivación a terapia intensiva y 36% en uso de asistencia respiratoria mecánica.
El ensayo clínico al que hace referencia el comunicado evaluó la seguridad y eficacia del suero en 242 pacientes hospitalizados con neumonía moderada (sin necesidad de suplementación de oxígeno) a severa (con oxígeno) por SARS-CoV-2 confirmada por PCR (121 recibieron el suero y 121, un placebo). Fueron enrolados en 19 hospitales y clínicas del área metropolitana de Buenos Aires, Neuquén y Tucumán. Tenían entre 18 y 79 años (con promedio de 54). Se administraron dos dosis del suero por infusión endovenosa (separadas por 48 horas) dentro de los diez días del inicio de los síntomas.
Una de las voces que lo desaprueban fue la del neurocientífico Pablo Richly, director del Centro de Salud Cerebral, que se mostró indignado en Twitter de que ningún periodista o medio haya dicho "nada sobre la falsedad de la supuesta reducción del 45% de mortalidad que se le adjudica al suero hiperinmune". También opinó que "Se necesita una buena explicación si se va a aprobar un medicamento con evidencia tan pobre que usualmente sería considerado escandaloso. Promoverlo con datos que no reflejan la realidad tampoco ayuda". Y más tarde agregó que "el problema no es el estudio, sino que haya sido aprobado por la Anmat".
Richly insistió en que "el objetivo primario del estudio (mejoría en escala de la OMS) no fue significativo (85% vs. 89%), tampoco el 'p-valor' ni los 'intervalos de confianza'. Tampoco hubo diferencias significativas en necesidad de asistencia respiratoria, ingreso a UTI o mortalidad. No se puede afirmar eficacia, probablemente por problemas del estudio y no de la droga. Pero para afirmar eso se requiere más investigación. Suponer eficacia es solo una hipótesis por el momento. Una muy costosa para el sistema de salud y para la confianza de la comunidad en los entes reguladores".
El infectólogo José Barletta dijo algo similar. Destacó que "los resultados primarios son interesantes, pero no permiten concluir lo que prometen. Hay una tendencia que parece que funciona, es un estudio generador de hipótesis, entonces lo que hay que hacer es otro estudio que pueda confirmarlas. Pero una vez aprobado, ya no va a ser posible reunir la evidencia porque no se va a poder ensayar contra placebo. La condición para su aprobación debería haber sido que se siguiera con el estudio de fase III".
Más Leídas
-
1
Llega el feriado del 1° de Mayo: ¿habrá fin de semana largo?

-
2
¡Saquen los paraguas!: a qué hora volverá a llover en Buenos Aires, según el pronóstico

-
3
Un crédito hipotecario sale al mercado en mayo: condiciones, montos y tasas que ofrecen

-
4
A los 60 años, se coronó como ganadora de Miss Buenos Aires 2024 e irá por el título nacional: la historia de Alejandra Rodríguez

-
5
Trenes de larga distancia: cuánto costará viajar a Mar del Plata, Córdoba, Rosario y Tucumán desde mayo

Suscribite a nuestro newsletter
Mantenete siempre informado
Notas relacionadas
También podría interesarte

Premier League: con un gol de Julián Álvarez, Manchester City goleó a un Brighton que tuvo a Valentín Barco de titular