A una semana de su arribo a la Argentina, 3,5 millones de vacunas de Moderna siguen guardadas en un depósito
Se trata de las dosis donadas por el gobierno de Estados Unidos. Desde Casa Rosada dicen que aguardan una autorización para su uso pediátrico.
Por Canal26
Jueves 22 de Julio de 2021 - 19:56
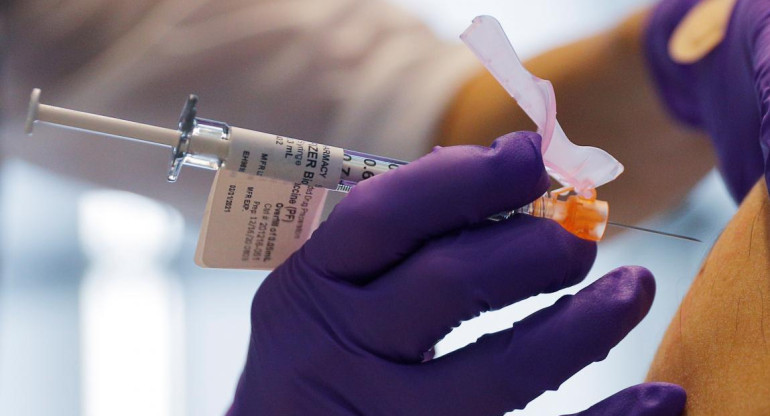
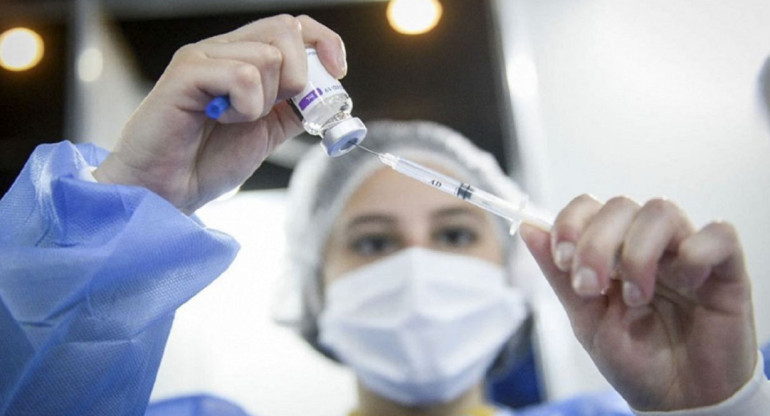
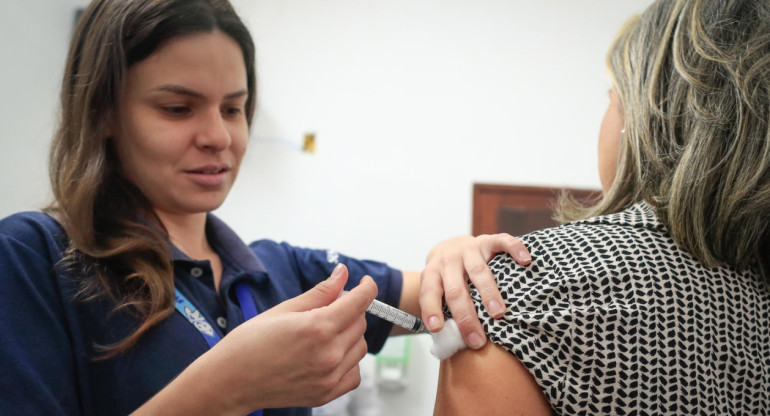
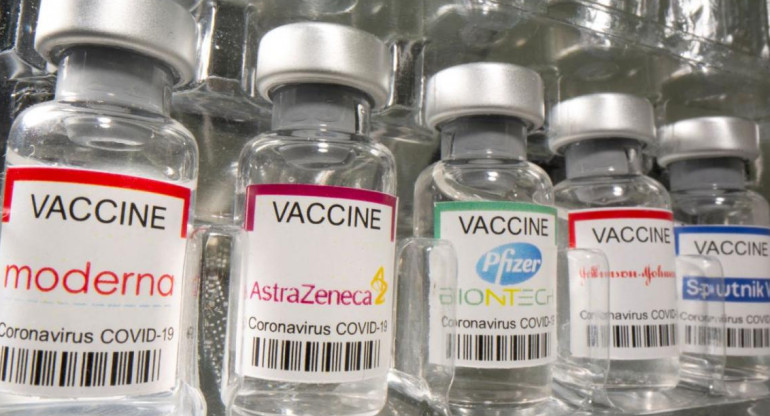
 Vacunas Moderna. Twitter: @USAmbassadorARG
Vacunas Moderna. Twitter: @USAmbassadorARG
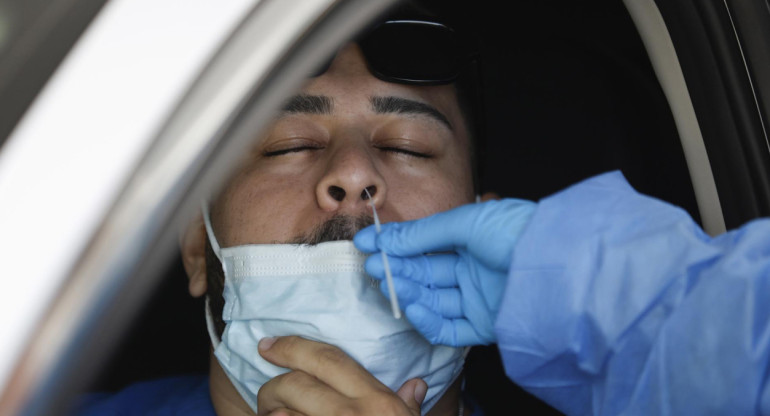
Tres millones y medio de vacunas de Moderna donadas por Estados Unidos y que llegaron la semana pasada al nuestro país, continúan guardadas en un depósito. El lote es la apuesta de la Casa Rosada para inmunizar de coronavirus a los menores de edad con comorbilidades, pero todavía no recibieron el aval necesario.
En ese marco, la ministra de Salud Carla Vizzotti, aseguró a principios de esta semana que “se encuentra próxima” la autorización para usarlas en menores de 18 años y las provincias confían en un proceso rápido por el acuerdo de reciprocidad entre la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) y la Administración de Medicamentos y Alimentos norteamericana (FDA, por sus siglas en inglés), el organismo que debe comunicar que esas vacunas son aptas para inocular a niños y adolescentes que tengan entre 12 y 17 años.
En resumen, hasta que esa aprobación no llegue, el Gobierno no aplicará las dosis. Otra alternativa para este grupo etario es que la ANMAT termine de analizar los informes que desde China envió el fabricante de Sinopharm para que esa marca de vacunas también sea de uso pediátrico. Se estima que entre 100 mil y 200 mil niños y adolescentes que padecen comorbilidades entrarán en una primera etapa de esa vacunación.
La donación de las vacunas de Moderna fue la más grande que Estados Unidos realizó en Latinoamérica. Al tratarse de una donación no se requiere registro de la vacuna de Moderna ante ANMAT, pero sí es necesario la autorización para su aplicación en el país.
La donación se llevó a cabo luego de que el Gobierno nacional aceptara adecuar la Ley de Vacunas 27.573 que también posibilitó que la Argentina firme el primer contrato de compra para vacunas de ARN mensajero a partir del primer trimestre del año 2022. Los ensayos en Fase III de la vacuna de Moderna mostraron una eficacia del 94% y una inmunidad de varios meses.
La vacuna de Moderna se almacena a -20 °C, lo que requiere el mantenimiento de la cadena de frío desde la fábrica hasta los centros vacunatorios. Una vez fuera de las heladeras, resiste hasta 30 días.
Desde el inicio del plan de vacunación en nuestro país, se han aplicado las vacunas Sputnik V, Sinopharm, AstraZeneca y Covishield, que es la misma de AstraZeneca, pero producida en la India.
Para autorizar o registrar vacunas, en nuestro país se utilizaron diferentes mecanismos. Uno de ellos es a través de empresas presentes en Argentina. Estas deben presentar información del desarrollo, producción y control de calidad, así como también los estudios clínicos que avalen la calidad, seguridad y eficacia requerida para su uso en humanos.
En el caso de Pfizer, vacuna que aun aguarda negociaciones entre el Ministerio de Salud y el laboratorio, la ANMAT había informado en diciembre que autorizó la inscripción en el registro de especialidades medicinales bajo la condición de venta bajo receta.
El organismo, también sacó otra disposición para autorizar la inscripción de la vacuna de AstraZeneca/Oxford. “Presenta un aceptable balance beneficio-riesgo, permitiendo sustentar el otorgamiento de la inscripción y autorización condicional del producto para la indicación solicitada. La misma se otorgó por el plazo de un año contado a partir de la fecha de la presente disposición, bajo la condición de venta bajo receta”, indicaba el comunicado.
En el caso de la Sputnik V, primero hubo una resolución del 24 de diciembre del Ministerio de Salud de la Nación y luego ANMAT hizo un análisis para la aprobación de su uso. En cuanto a la Sinopharm, se autorizó también a partir de una resolución del Ministerio el 22 de febrero pasado. En ambos casos, la autorización de uso de emergencia de las vacunas se encuadraron en el marco de la Ley 27.573.
Más Leídas
-
1
Cadena nacional de Javier Milei: el superávit fiscal, el "fin del supuesto Estado presente" y otras definiciones

-
2
Cristina Kirchner en la previa de la marcha universitaria: "Educación pública para la igualdad de oportunidades"

-
3
Ignacio Zuleta analizó la actualidad argentina en "La Mirada":

-
4
Javier Milei calificó de “héroes” a quienes fugaron dólares: “Escaparon de las garras del Estado"

-
5
Nardini estuvo en el comienzo del ciclo lectivo del CDI de Ingeniero Adolfo Sourdeaux

Suscribite a nuestro newsletter
Mantenete siempre informado
Notas relacionadas
También podría interesarte

La inteligencia artificial responde: ¿cuál es el libro más importante en la historia de la humanidad?