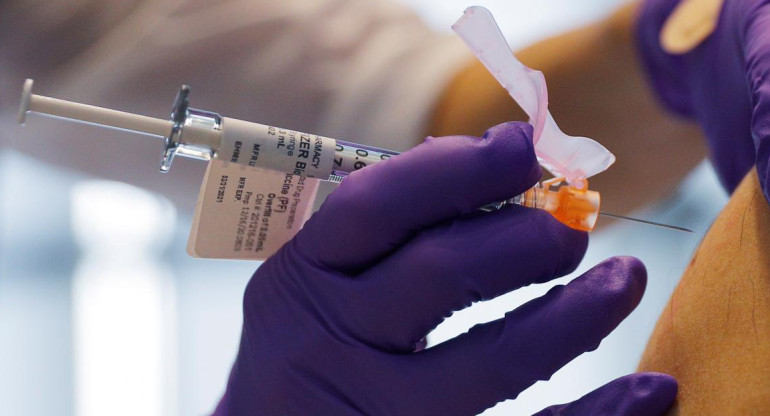
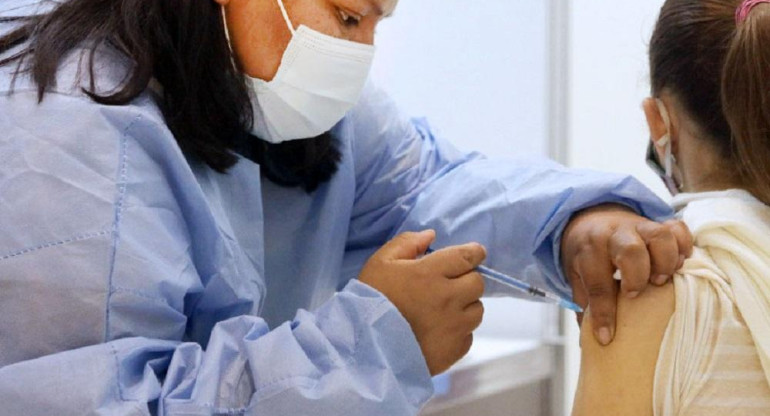
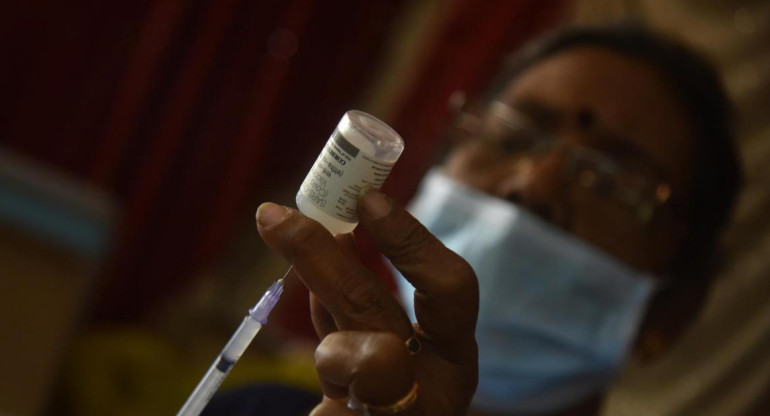
Claves de vacuna argentina contra el coronavirus
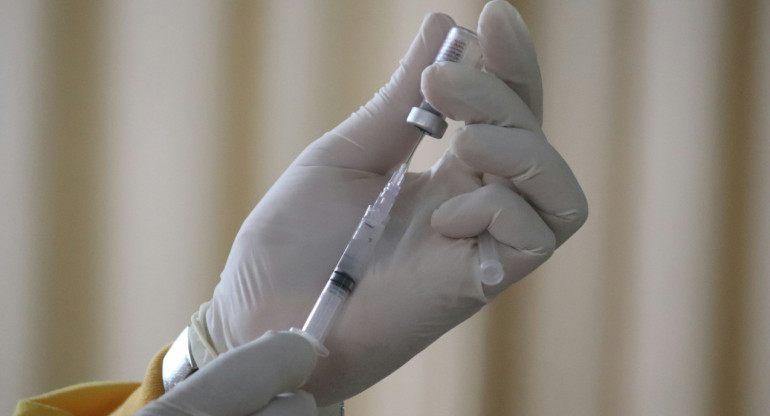
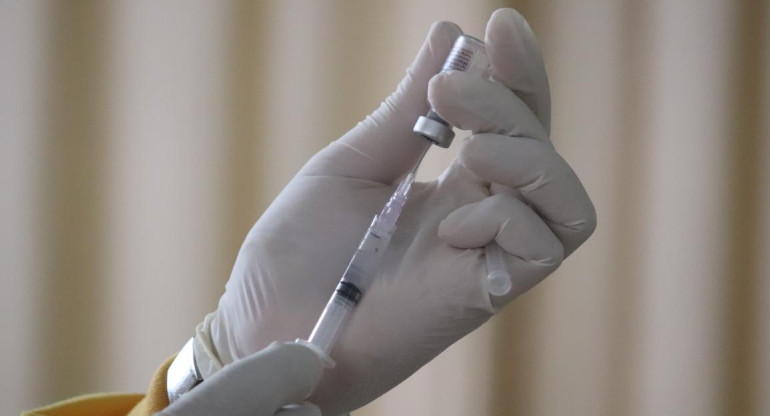
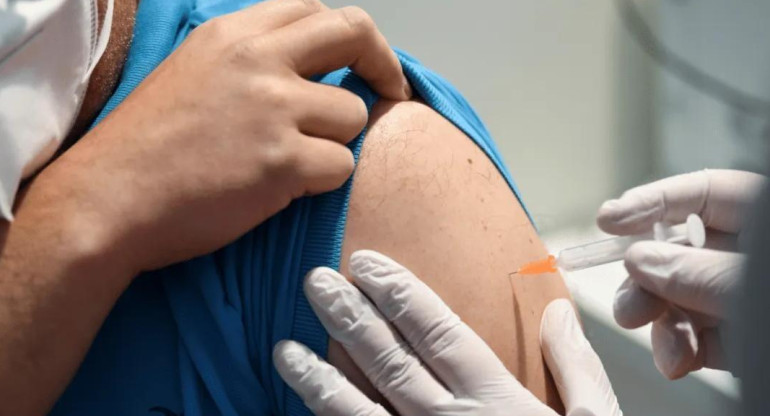
"Arvac-Cecilia Grierson" está basada en proteínas del coronavirus que se elaboran y sintetizan en el laboratorio. El desarrollo comenzará a probarse en humanos: participarán 80 voluntarios sanos que ya hayan recibido un esquema de vacunación completo.
Por Canal26
Viernes 1 de Abril de 2022 - 07:02
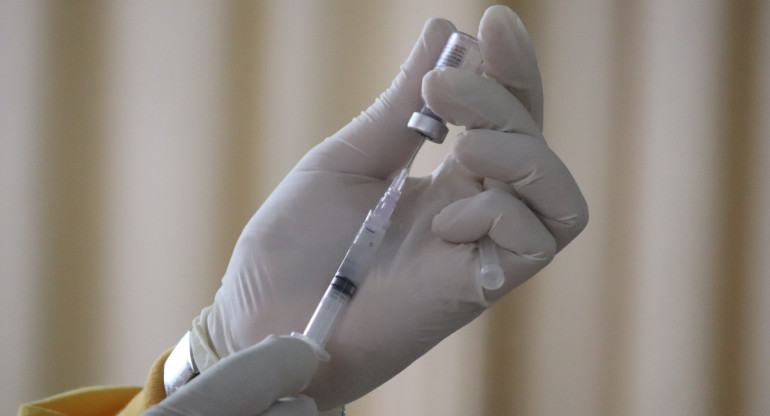
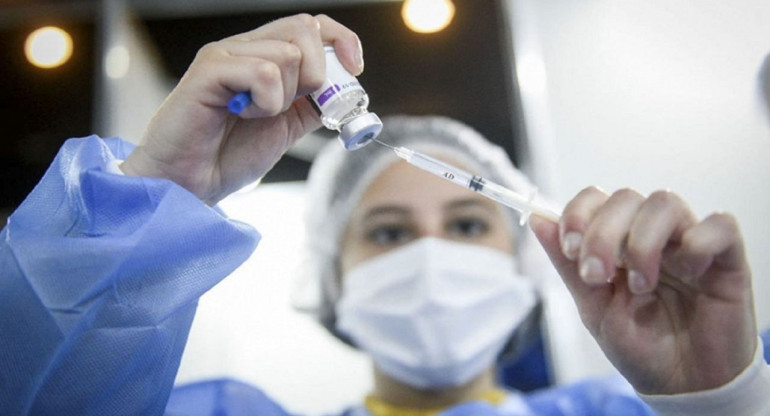
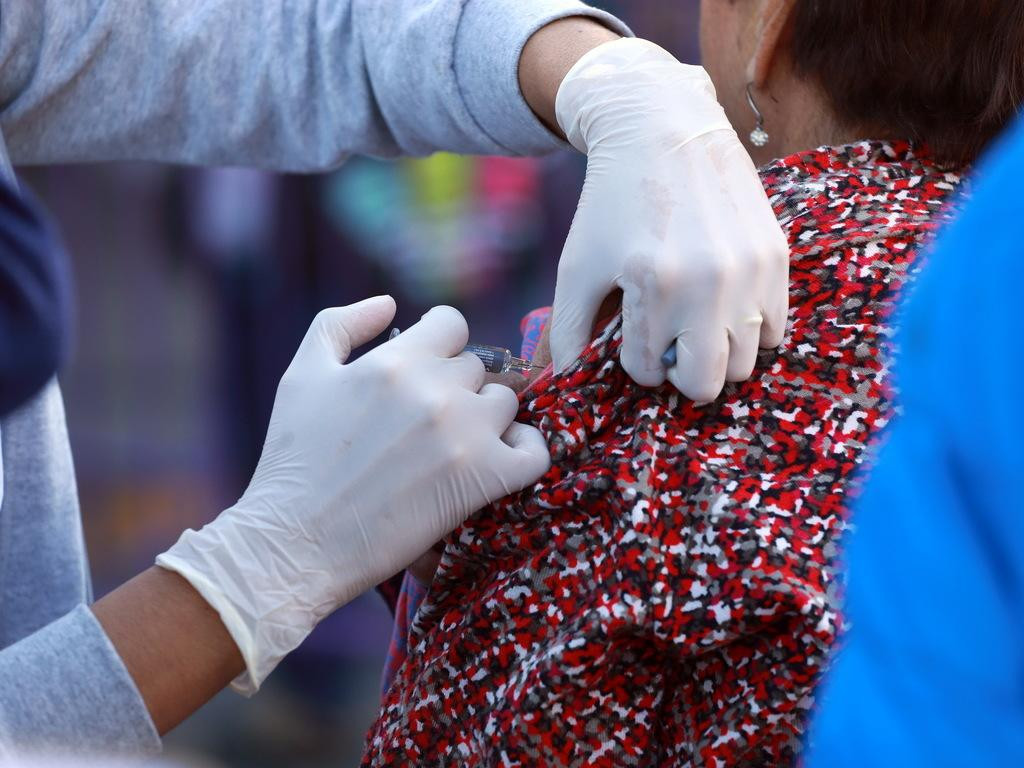 Foto NA.
Foto NA.
La vacuna "Arvac-Cecilia Grierson", basada en proteínas del coronavirus que se elaboran y sintetizan en el laboratorio y que comenzará a probarse en humanos, “podrá producirse en nuestro país de punta a punta y servirá para aprender a trabajar de nuevas formas y para futuros desarrollos", señaló la líder del proyecto, Juliana Cassataro.
"Arvac-Cecilia Grierson" comenzó a desarrollarse por el grupo liderado por Cassataro de la Universidad de San Martín (Unsam) y el Conicet en junio del 2020 y los estudios preclínicos fueron financiados por la Agencia Nacional de Promoción Científica (Agencia de I+D+i), dependiente del Ministerio de Ciencia, Tecnología e Innovación.
En tanto, el desarrollo y escalado industrial, así como el estudio clínico de fase 1, son financiados por el Laboratorio Pablo Cassará.
Un día después del anuncio de que la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (Anmat) aprobó el inicio de pruebas en humanos (Fase 1) de la vacuna, Cassataro dialogó sobre los detalles técnicos, la elección del nombre, lo que implica la vacuna para el país y cómo ejercen los liderazgos las mujeres.
"La vacuna que desarrollamos se basa en producir y purificar de forma sumamente controlada una proteína (un partecita) que forma parte del virus SARS-Cov-2, y que introducida en el organismo actuará como antígeno contra el cual el sistema inmunológico de las personas desarrollará anticuerpos", reveló.
Otras tecnologías más novedosas también se basan en elaborar antígenos que desarrollan anticuerpos contra una porción del virus, pero mientras que en las vacunas de RNA mensajero o vectores virales el antígeno es producido por el propio cuerpo mediante la introducción de material genético en nuestras células, en el caso de las proteínas recombinantes el antígeno es producido y purificado en el laboratorio farmacéutico con procesos sumamente controlados y validados, sin introducción de material genético en el organismo.
Es además una tecnología que puede tener menor costo de producción que las demás y es de fácil transferencia tecnológica porque hay muchos lugares que producen proteínas recombinantes; esto quiere decir que se puede producir en muchos lados. Por otra parte, puede guardarse en la heladera y esto podría hacer más fácil la distribución de las vacunas.
"En esta fase 1 participarán 80 voluntarios sanos que ya hayan recibido un esquema de vacunación previo completo, que no hayan recibido refuerzo y que no hayan tenido Covid en los últimos dos meses. El objetivo principal de esta fase es comprobar la seguridad y el tiempo estimado de duración es de tres meses", manifestó.
"En ese sentido sería la primera vez que una vacuna preventiva diseñada en una universidad pública llega a realizar ensayos de fase 1, es un hito para todo el sistema público de ciencia y tecnología; cada paso nos va a servir para generar en esta y otras vacunas nuevos desarrollos y nuevas formas de trabajar. Es un paso muy importante de un largo camino", dijo.
"En este contexto es importante destacar que el proyecto comenzó a avanzar más rápido cuando los investigadores de la universidad nos vinculamos con los de la empresa Laboratorio Pablo Cassará que tenían más claro el tema regulatorio. Quienes hacemos investigación básica no tenemos esas cuestiones tan en mente, en eso es clave la existencia de investigadores en empresas biotecnológicas que tienen esa mirada", cerró.
Más Leídas
-
1
Descubren una sorprendente pirámide antigua sumergida en las profundidades del océano

-
2
Cronograma de pago ANSES: quiénes cobran este miércoles el bono de $70 mil de abril

-
3
ANSES confirmó un bono de hasta 91 mil pesos para un grupo de beneficiarios: quiénes pueden cobrarlo

-
4
¿Qué significan las zapatillas colgadas de los cables?

-
5
Llega el descanso: cuándo son las vacaciones de invierno 2024 en cada provincia

Suscribite a nuestro newsletter
Mantenete siempre informado